博腾生物是一家端到端的基因与细胞治疗CDMO服务,我们提供技术转移,工艺开发,分析方法开发,cGMP生产,检测服务和发现研究,包括专有技术许可,涵盖不同的细胞和基因治疗领域。

博腾生物拥有知识和经验丰富的工艺科学团队,提供灵活、多选的工艺开发路线以满足客户在不同药物开发阶段的需求,覆盖临床前,临床I期,II期和III期以及商业化阶段。
对于已经拥有工艺, 仅有临床和商业阶段生产需求的客户,我们可以提供头对头的技术转移服务并支持大规模生产。我们帮助在临床III期的项目进行工艺表征和验证(PPQ),以支持NDA和商业化生产。最后,对于处于临床前和早期临床研究阶段的客户,我们提供全流程工艺开发,优化和放大,及GMP生产支持。
高效的技术转移是药物开发过程中的关键环节。在博腾生物,我们建立了明确的技术转移流程,从原料,细胞库,上下游工艺,原液/成品生产等差距分析开始,针对药物的关键质量属性(CQA)进行上下游生产和工艺设备及参数的分析与评估。我们的专业技术转移团队将进行深入评估,以确保分配适当的资源,平衡开发时间和成本,并在不影响质量的情况下实现按时交付。
与工艺开发团队类似,分析研发团队能够对客户转移过来的分析方法进行优化或进行分析方法的完整开发工作。
我们的分析研发团队具有专业的分析研发技能,对细胞治疗产品、病毒载体、溶瘤病毒、mRNA及质粒产品等在鉴别、含量、纯度、活性及安全性等方面具有丰富的开发经验,并已建立了200个以上的平台分析方法。
对于客户已建立的分析方法,我们将在遵从客户方案和符合法规要求的基础上,对分析方法进行转移和验证/确认。
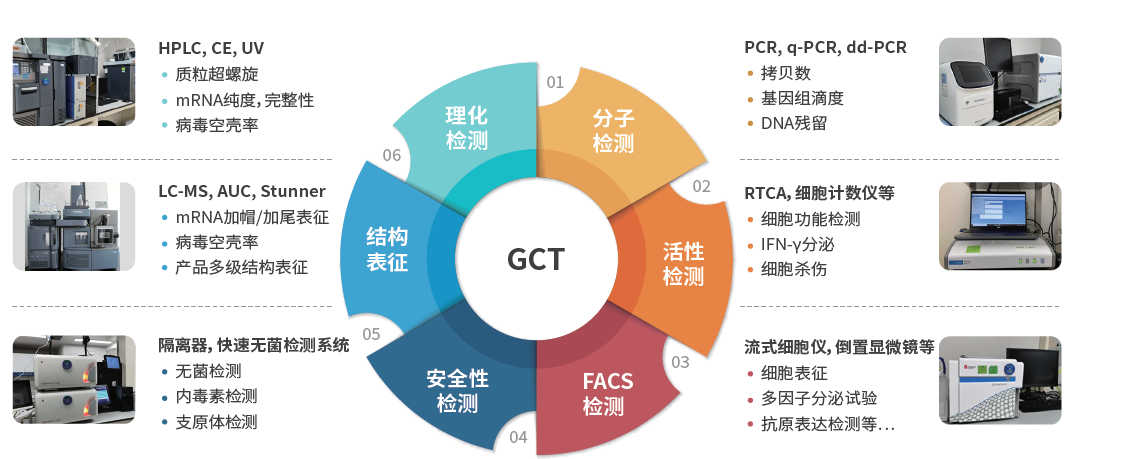
我们的分析研发实验室配备了大量先进的仪器设备,分析研发团队具有优秀的专业技能且在各领域具有丰富的分析方法开发经验,如分子学、细胞分析、蛋白质组学、生物学、生物化学等;我们将DoE应用于分析方法的开发和优化中,建立了针对产品和工艺过程样品的诸多方法,涵盖活性类、鉴别类、含量与纯度类、安全性等分析方法。
超螺旋比例是质粒转染有效性的一个关键指标。图10展示了采用阴离子交换色谱检测质粒超螺旋比例的色谱图,图中显示开环和超螺旋峰可以良好的分离。
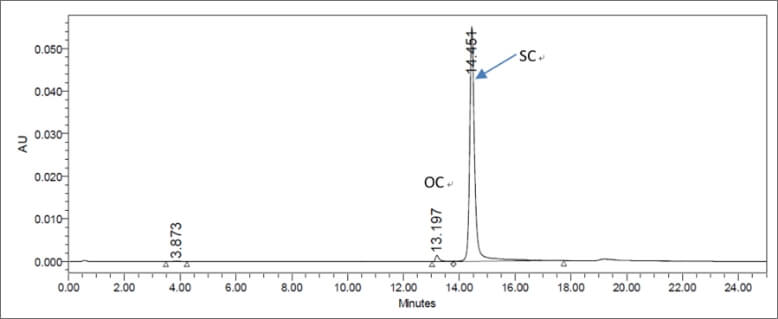
图10 代表超螺旋质粒的IEX-HPLC色谱图(SC:超螺旋,OC:开环)
根据法规要求,慢病毒产品中不应含有长度大于200bp的DNA片段。我们开了采用毛细管电泳仪检测DNA片段大小的分析方法,如图11所示。LV产品的图谱与质控标准相比,可以看出LV产品中没有200bp以上的DNA片段。
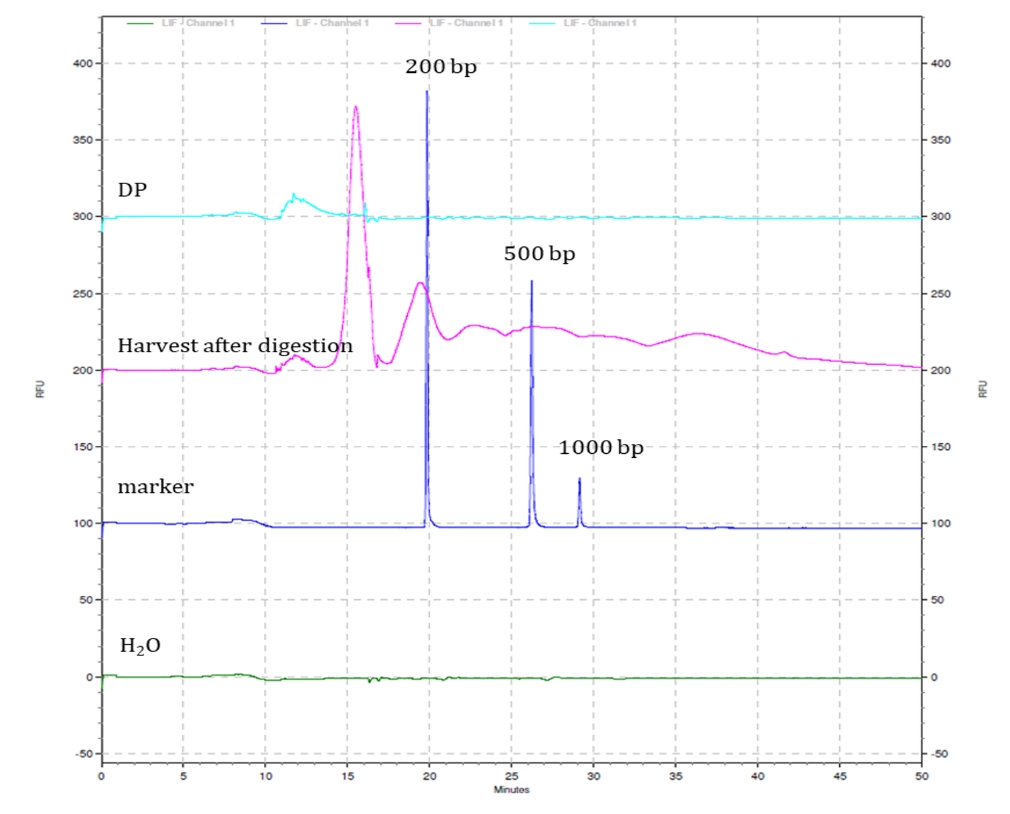
图11
通过CE-LIF采集得到的LV产品的DNA片段分布电泳图
多种因素会影响CAR-T细胞产品及持久性,包括细胞的纯度、功能、增殖和持久能力(如图12)。我们的分析研发团队可以为CAR-T细胞的工艺生产过程进行实时检测和监控。我们开发了最先进的分析方法,这样可以同时进行多个细胞表面标记物、细胞内、核蛋白的染色分析。
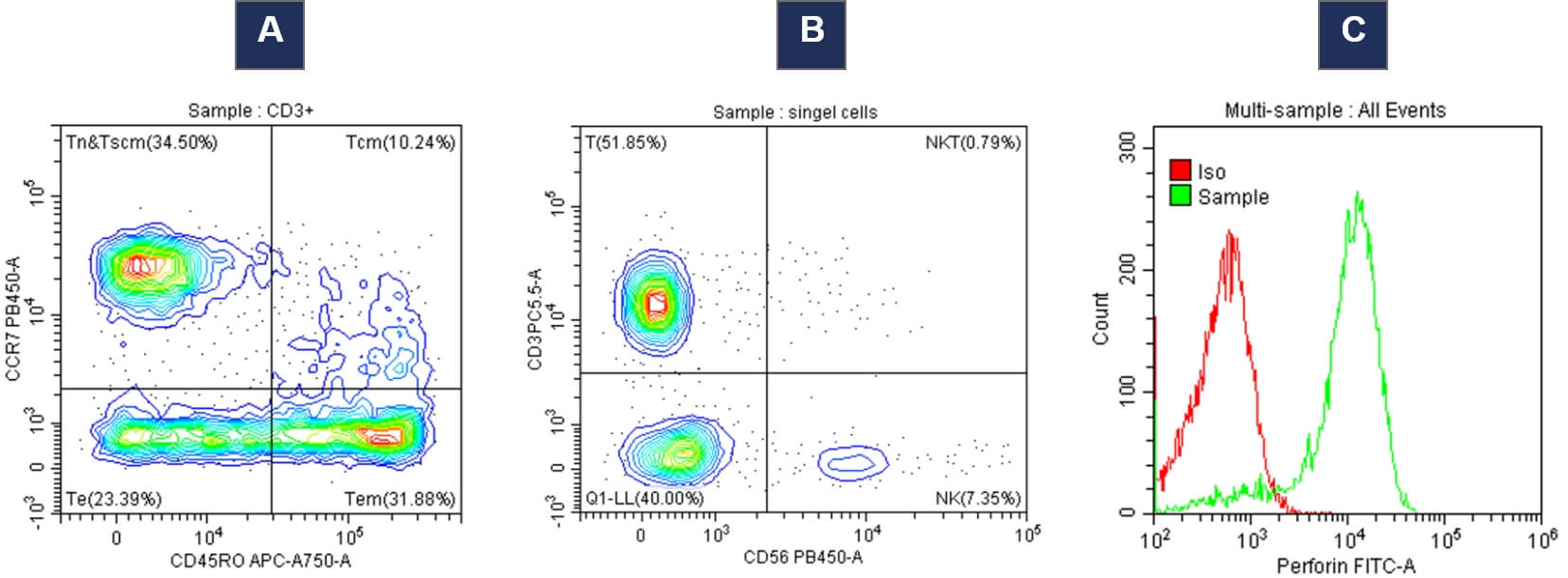
图12 A&B图展示了通过FACS检测的PBMC的免疫表型,C图展示了NK细胞的免疫表型。在A和B图中,通过对细胞表面marker(如CD3、CD56、CCR7、CD45RO等)染色去分析NK和PBMC细胞中的记忆T细胞亚群。图C展示了NK细胞中穿孔素(perforin)的表达。perforin是自然杀伤细胞和杀伤性T细胞介导靶细胞裂解的的一个主要的效应分子。
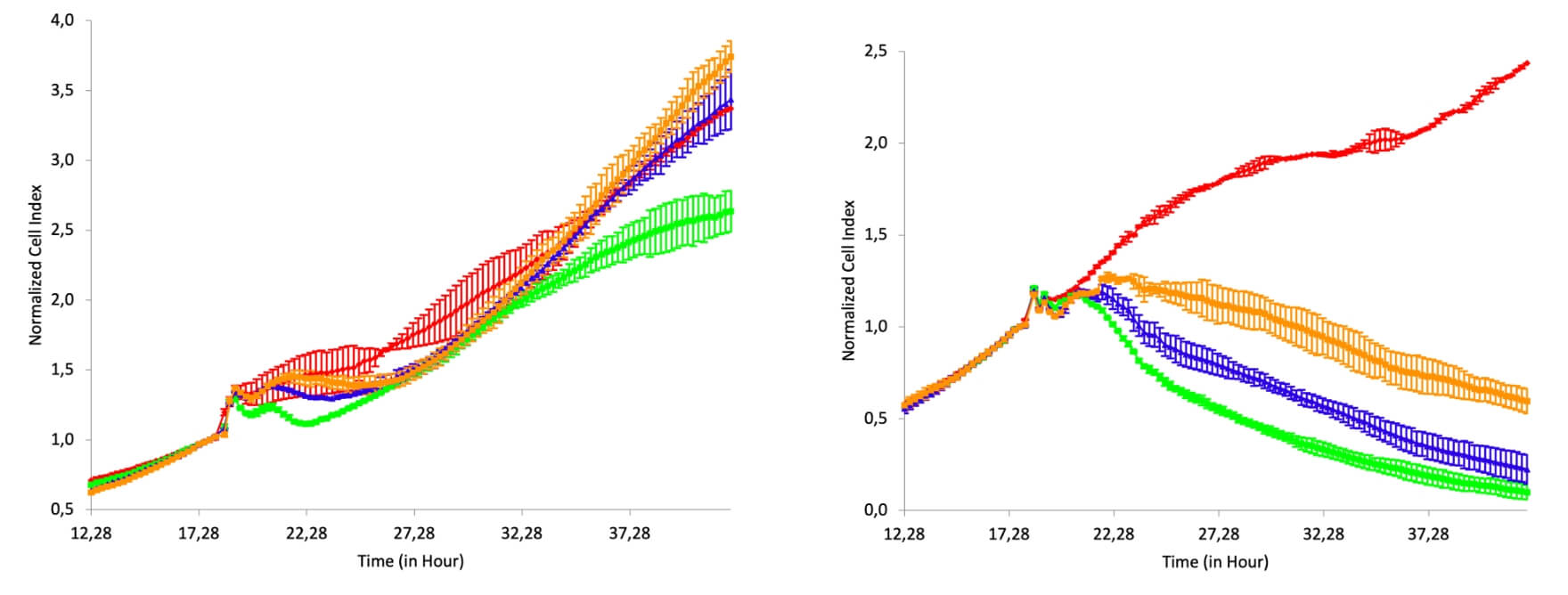
图13 使用RTCA(实时细胞分析仪)设备来监测CAR-T细胞实时杀伤功能
高空心率的AAV产品会降低产品的感染效率,同时带来免疫原性
因此,需要监控AAV产品的实心率以保证产品的有效性和安全性;图14展示了采用SEC-MALS法(体积排阻色谱结合光散射仪、UV检测器和RI检测器)检测病毒实心率的色谱图。
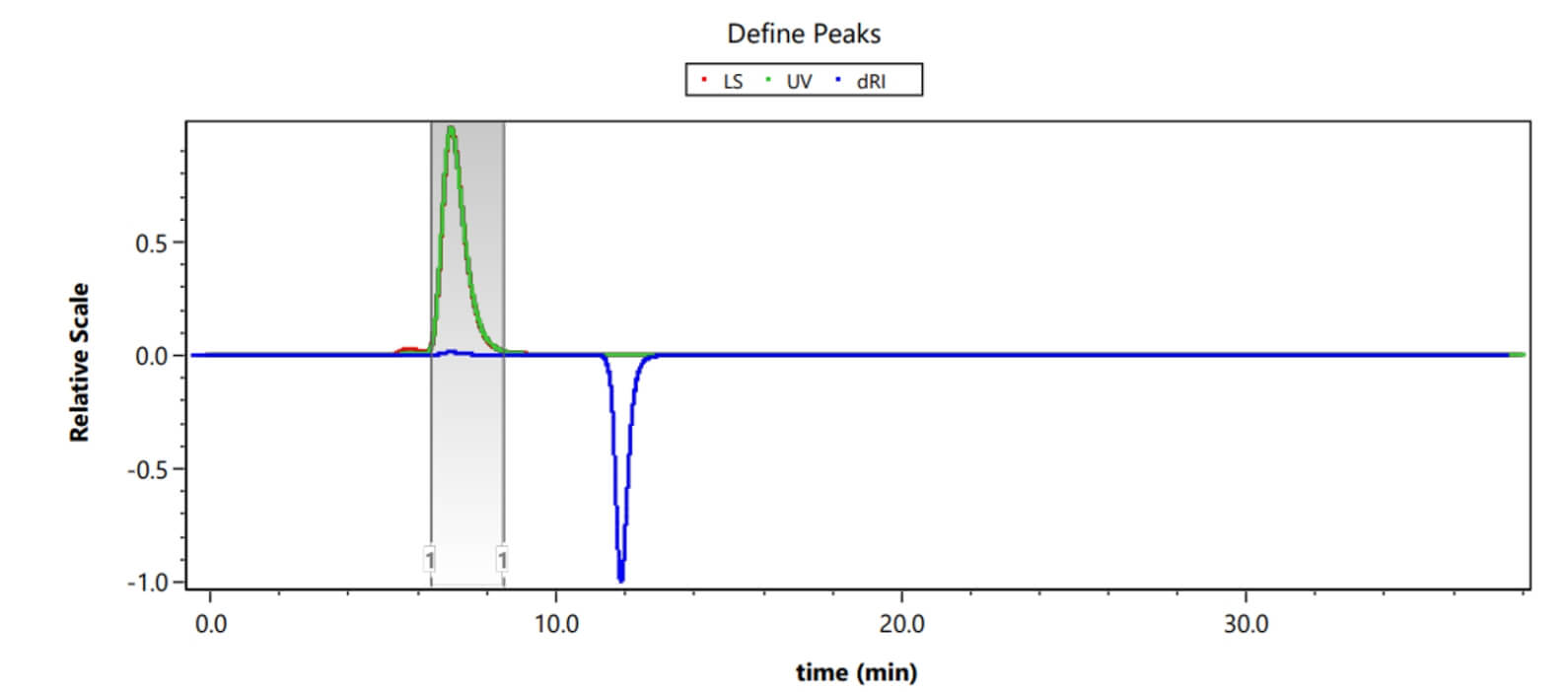
图14 采用SEC-MALS法检测AAV的实心率
AAV病毒颗粒容易聚集并且产生聚集体,这些聚集体会导致AAV产品的感染效率降低,同时带来安全风险,所以需要对AAV产品的粒径分布进行检测。
我们的分析研发团队采用Stunner设备开发建立了AAV病毒颗粒粒径分布的分析方法,如图15所示。
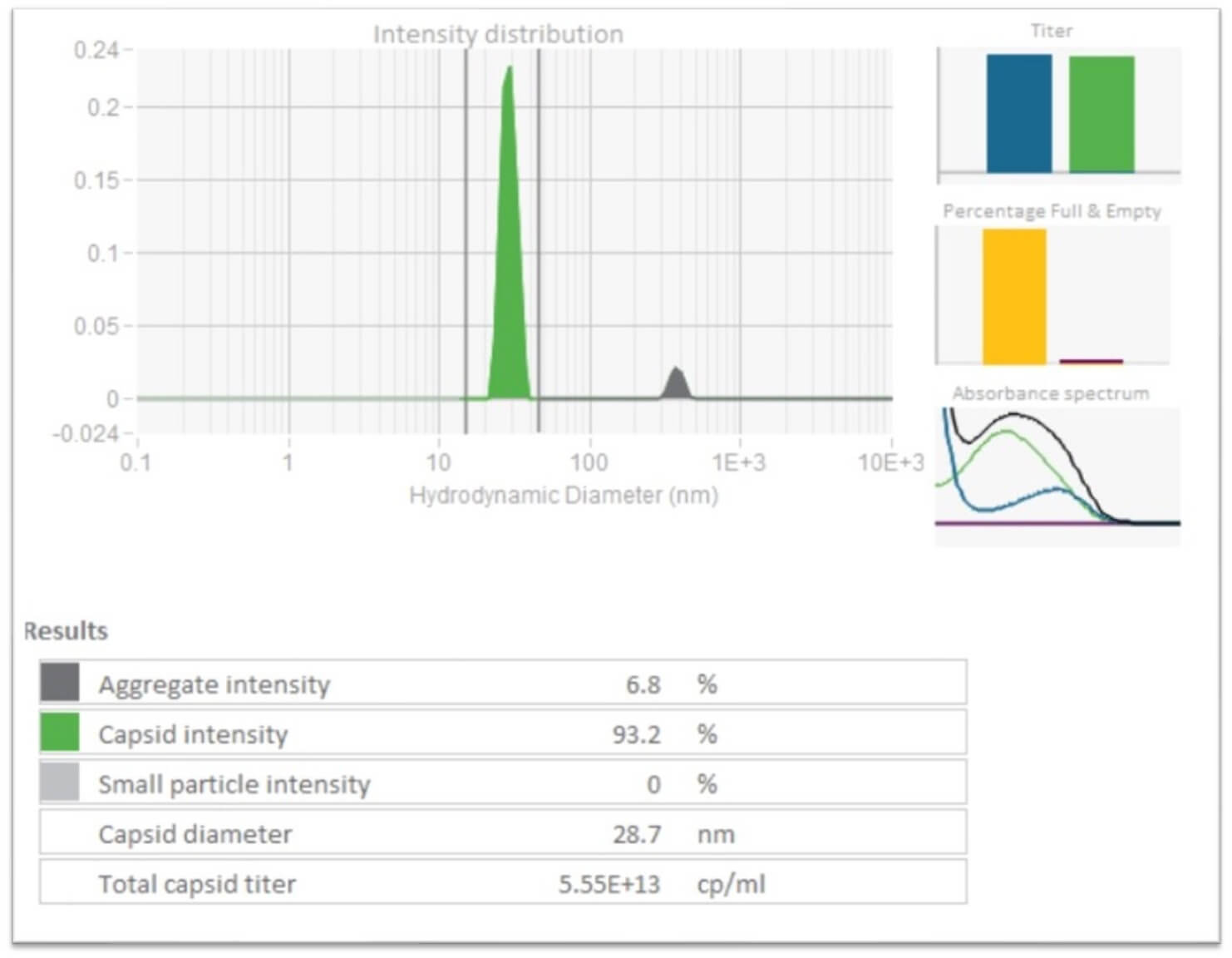
图15 采用Stunner设备检测AAV的粒径分布
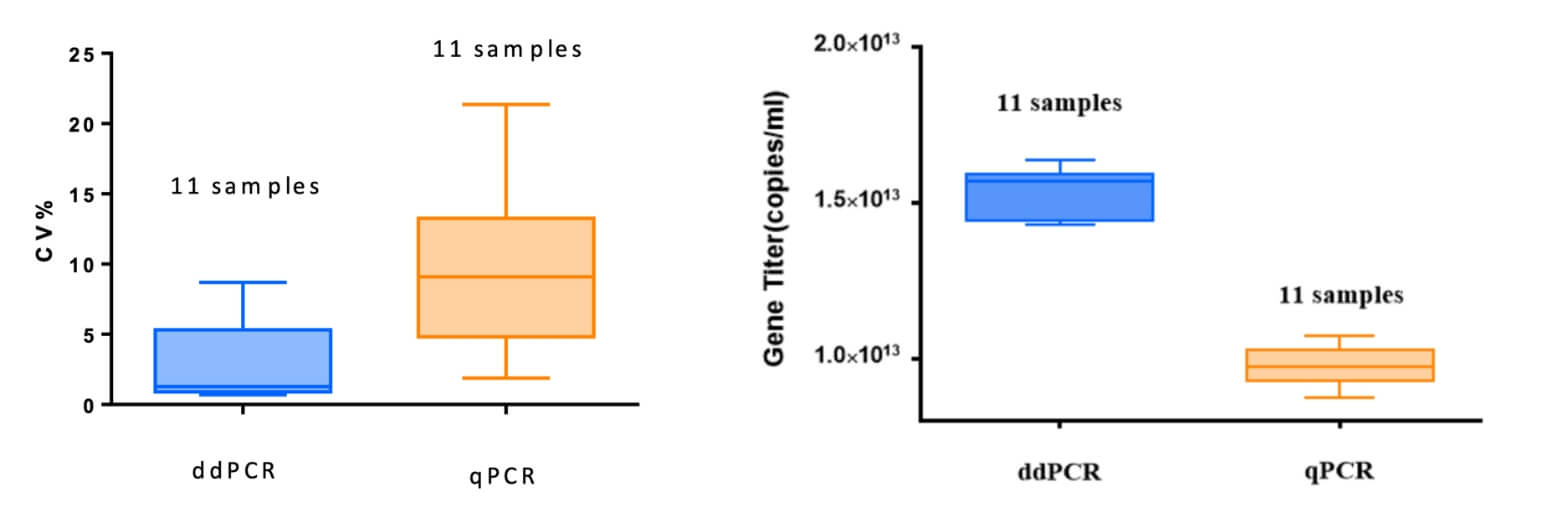
AAV的基因组滴度是用来确定产品剂量的重要方法,常用的检测手段报告QPCR法和ddPCR法(如图16A和B)。ddPCR是一种绝对定量方法,与QPCR相比,具有更好的准确度和精密度。
我们为客户提供ddPCR和QPCR的分析方法开发服务,以满足客户的不同需求。
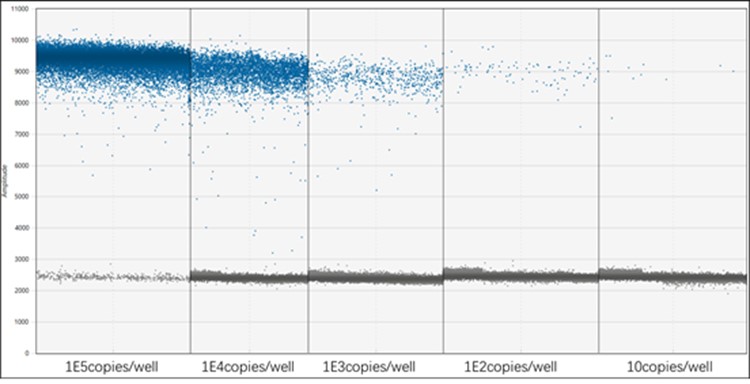
图16A 采用ddPCR检测AAV基因组滴度的检出限为3拷贝,相对定量下限为20拷贝,相对定量上限为1E5拷贝
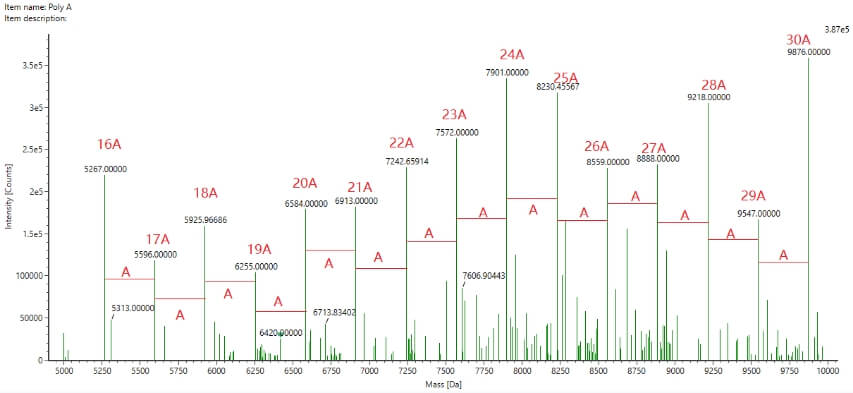
Poly A尾长度影响产品的稳定性和功能。
在博腾生物,我们已经开发了LC-MS(高效液相色谱与质谱联用)的方法用于poly A尾的表征。
我们通过先进的16000平米GMP厂房来帮助客户进行临床试验和商业化阶段的基因与细胞治疗药物cGMP生产。
我们的技术和生产能力得到了客户的广泛认可和重视,特别是端到端的支持能力,包括质粒生产,细胞库/毒种库建库,原液 /成品生产和灌装。我们提供non-GMP和GMP生产,以满足客户在临床前或临床和商业化阶段的不同需求。我们的 GMP 车间符合BSL-2标准,按照不同洁净等级管理(B级间+C级间),可进行质粒、病毒载体和细胞的生产。

在开启细胞和基因治疗生产项目时,建立作为起始材料的高质量GMP主细胞库和毒种库至关重要。我们在细胞库/菌种库建方面的经验能够更好地为客户服务。我们的团队擅长细胞和菌种库建库、工艺表征、克隆筛选和GMP生产。
我们对于不同细胞系生产系统都有着丰富经验,包括HEK293/T,HeLa,SF9,Vero,A549等。我们提供从基于质粒的系统中从头开始生产和回收传染性病毒颗粒,以及遗传表征、克隆优化和种子筛选,以初步优化病毒传染性和滴度。

我们为病毒载体、细胞治疗及mRNA原液和成品提供non-GMP和GMP生产服务。我们所有的创新生产平台都符合国际监管机构的要求,包括FDA,EMA,NMPA等。我们还为提交 IND 和 NDA 提供 CMC 监管支持。
在细胞治疗方面,我们已经为自体和异体细胞治疗平台建立了稳健的GMP制造工艺。目前,我们有十几个CAR-T细胞治疗生产模块。我们为non-GMP和GMP生产提供端到端支持,从质粒到慢病毒,再到细胞治疗产品生产。
对于基因治疗,我们建立了创新和强大的AAV和慢病毒载体制造平台。我们提供HEK293和SF9生产平台,用于不同生产规模的non-GMP和GMP生产。我们拥有多达十条病毒载体生产线,使我们能够根据客户的需求定制工艺方法,包括贴壁和悬浮系统。
我们还拥有专门的团队和生产模块用于溶瘤病毒疗法的制造。我们的病毒制造能力和能力可以满足临床前、临床和商业化阶段溶瘤病毒疗法的需求。我们新建立的mRNA GMP生产模块使我们能够为GMP mRNA生产提供端到端支持,包括质粒GMP制造和线性化,mRNA体外翻译,上游生产种的加帽和加尾,下游生产中的多步骤纯化以及研究级别的LNP包封和灌装。
我们拥有十几个质量控制 (QC)实验室以提供完整的 QC 检测服务,用于所有基因、细胞和病毒载体治疗的原液和成品的放行检测。我们强大的质量控制能力对原液和成品生产至关重要,最终确保患者安全并从治疗中获得最大收益。

我们的加工生产线能够每小时生产多达3000支,每批生产20000支。我们可以提供独立的灌装服务,或者作为整体服务的一部分提供灌装服务。
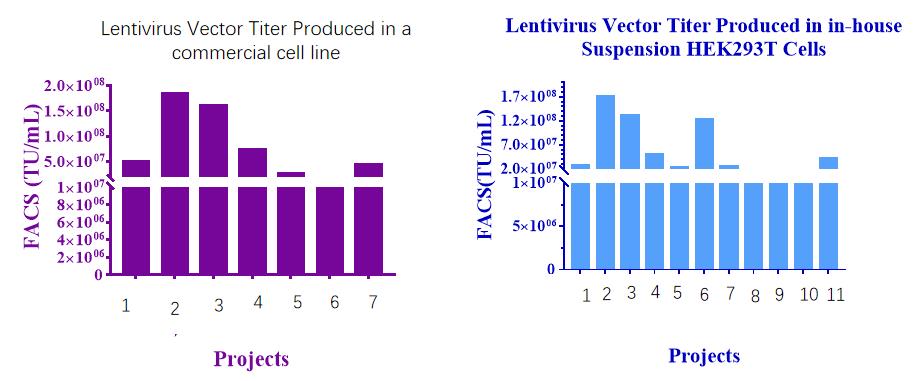
两种悬浮细胞慢病毒包装系统的病毒滴度:
A. 商业化慢病毒包装系统,B. PTLV-SMART慢病毒包装系统
图4
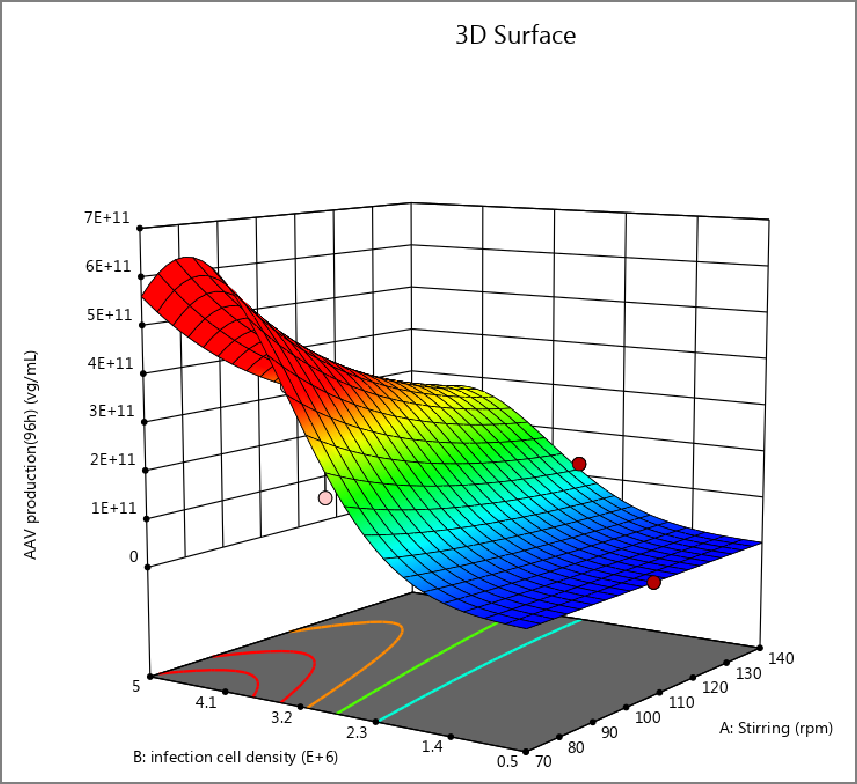
图9
DOE法优化AAV生产工艺参数。(此时最优参数:搅拌速度:70~140rpm;细胞密度:4.10E+06 cells/mL;模型预测结果:6.33E+11 vg/mL)

AAV 变体在文库筛选过程中在不同组织中富集。将准备好的AAV 文库并注射至宿主。两周后,收集组织并分离病毒基因组用于 PacBio 测序。病毒基因组富集于不同的组织中。
图18

通过我们文库筛选出的 AAV 变体,该病毒可包装 6.1kb 的基因组。
图19
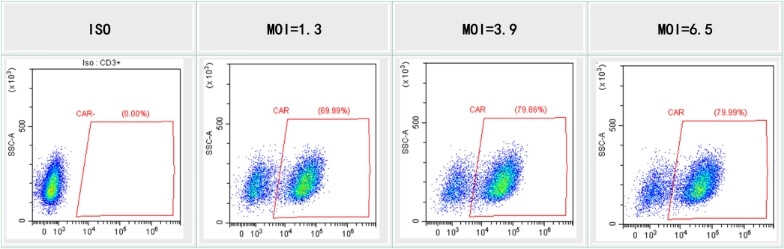
使用我们的HEK293T系统生产的慢病毒进行T细胞转导。T细胞在不同的MO下感染慢病毒,通过FACS测量CAR-T细胞百分比。
图 20
