合规从“0”开始:符合GMP、满足中美双报的现货PBMC
诱导多能干细胞(iPSC)技术正深刻重塑再生医学的发展格局。从疾病建模、药物筛选到细胞治疗,iPSC已在眼科疾病、心血管疾病、神经退行性疾病及肿瘤免疫等多个领域取得早期临床成功。截至2025年,全球已有数十项iPSC临床研究发表,百余例患者接受治疗;2026年2月,两款iPSC细胞疗法药物获批上市——这场医学革命,已从实验室加速迈向商业化。
然而,对每一位iPSC药物开发者而言,研发管线的每一步都面临现实拷问:时间、成本与合规,如何兼得?起点,往往决定终点。在iPSC药物开发中,细胞来源的选择,直接影响着重编程的效率与安全性。
PBMC(外周血单个核细胞)凭借微创获取、基因组稳定、供者普适性强等优势,已取代皮肤成纤维细胞,成为公认的“黄金原料”。在此基础上,如何快速锁定符合中美双报标准的高质量PBMC,成为加速药物研发的关键一环。
相较于侵入性强的皮肤活检或异质性高的间充质细胞,PBMC仅需10 mL静脉采血即可获得,且不受供者年龄限制,已成为规模化生产与自体/异体细胞治疗的理想起点。但值得注意的是:并非所有PBMC都具备“临床级”资质。细胞活率低、批次差异大、供者背景不明确——任一环节的瑕疵,都可能成为重编程失败或监管审评的隐患。
面对中美双报的严苛监管环境,细胞来源的合规性与可追溯性已成为药物开发者面临的第一道关卡。从CDE到FDA,监管机构对起始细胞的要求,正在从“可用”升级为“可溯、可查、可控”。
正是在这一背景下,博腾生物联合合佑生生物率先推出符合GMP及中美双报标准的PBMC,真正从源头为iPSC重编程构筑起坚实的合规基石。所谓“从‘0’开始”,不仅意味着在研发起点即规避合规风险,更代表双方已构建起一套贯穿供体筛选、样本采集、分离制备、质量控制全流程的完整合规闭环。
符合中美申报的PBMC全流程完整体系赋能
1、合规伦理审查
· 准备中英文对照的伦理上会文件,满足FDA申报资料提交要求;
· 采用符合FDA标准的供者筛查问卷及知情同意书模板;
· 设计适用于供者细胞商业化用途的知情同意书;
· 在GCP管理规范框架下开展审查工作;
2、供者筛选与筛查
· 供者知情同意过程现场可追溯;
· 供者国籍选择符合中美两国相关法律法规要求;
· 传染病筛查检测采用申报要求所规定的方法与内容;
· 传染病筛查流程符合CLIA标准;
· 开展血型及HLA分型检测;
· 明确传染病检测的窗口期设定;
3、样本采集与运输
· 样本采集过程具备可追溯性,所用设备均经过验证;
· 样本暂存与运输环节均经过验证,全程可追溯;
4、PBMC分离制备
· 在GMP环境与体系下完成分离制备操作;
· 分离及冻存工艺均经过验证;
5、PBMC质量控制
· 开展无菌、支原体及内毒素检测;
· 进行流式细胞表型分析;
· 完成细胞数量与活率检测;
· 进行全基因组(WGS)及全外显子组(WES)测序。
从供体筛选、样本采集、分离制备到质量控制放行,每一个环节均严格遵循中美双方法规的最高标准,博腾生物联合合佑生生物制备的PBMC产生的药效数据、安全性评价及质量控制结果,能够在申报资料中无缝对接,避免因样本源头合规性问题导致的发补风险,为您的全球研发战略赢得宝贵时间。
PBMC在中美双报中的审评差异及对比分析
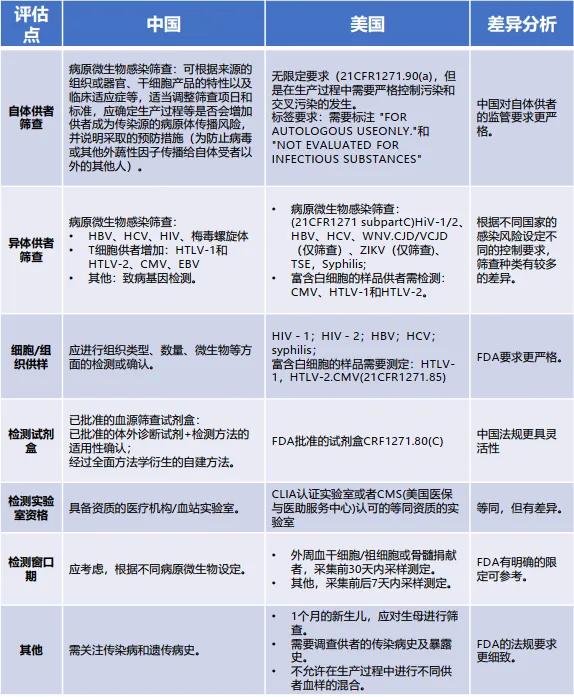
捐赠者筛查检测详情(FDA审核标准)请查看链接:
符合GMP及中美双报的PBMC优势
01源头合规,可追溯的合规完整文件链
针对中美双报,细胞来源的可追溯性与合规性是首要关卡。合佑生生物已建立丰富稳定的中外人群健康供者资源库,可为客户提供法规解读、政策分析、内资认定、国合审批等完整的合规审批流程服务。
合佑生生物建立了符合中美法规要求的完整文件链。从《供体知情同意书》《伦理审查批件》,到《采集/分离记录》《放行检测报告》及《稳定性数据》,合佑生提供全生命周期的文档支持,确保在面对监管机构核查时,每一份样本都有据可查、有源可溯。
02节约时间和成本,让研发周期“做减法”
低质量的起始细胞是工艺开发中的“隐形杀手”——它可能导致重编程效率低下、实验反复失败,无形中消耗有限的研发经费。与其耗费数月筛选供体、建立分离质控体系,不如直接启用经过验证的“现货”资源。该PBMC产品经严格的供者筛查、分离制备、质量检测及基因测序,确保符合CDE与FDA申报要求,使团队可直击重编程工艺开发核心环节,将研发资源聚焦于下游分化与功能验证。
03双重质检体系,中英文报告可直接用于申报
依托博腾生物高质量的GMP生产体系,确保每批次出厂PBMC均具备稳定均一的质量。
博腾生物生产制备的每一批次PBMC均同时进行中美双报要求的全套质控检测,包括但不限于无菌检查、支原体检查、内毒素检测、细胞活率及CD3+/CD4+/CD8+等关键免疫细胞亚群的流式细胞术分析。我们出具的检测报告支持中英文双语,可直接作为申报附件材料。
我们提供的不止是符合中美申报的PBMC细胞,更是全流程赋能的系统能力。
关于博腾生物
苏州博腾生物制药有限公司成立于2018年12月,立足苏州,以上市公司-博腾股份(股票代码:300363)为依托,为全球客户提供基因与细胞治疗药物从临床前研究到药品上市全生命周期所需的一站式服务解决方案。
博腾生物建立了质粒、病毒载体、细胞治疗、基因治疗、核酸疗法等CRO和CDMO平台,拥有总面积超过20000m2的研发与生产基地、10条病毒载体生产线、12条GMP细胞治疗生产线(含2个商业化生产车间),以及上百个洁净车间。截至目前,博腾生物已助力客户在全球范围内获得24个临床批件,覆盖中国、美国、新西兰等国家,已有11个临床I期/II期及商业化工艺变更阶段项目,并成功帮助多个海外项目转化到中国。我们致力于以客户为中心,为客户提供卓越的全球化、端到端CDMO服务,让好药更早惠及大众。
关于合佑生生物
无锡合佑生生物科技有限公司是一家专注原代细胞及相关试剂与技术服务的创新型生物科技企业。团队长期深耕细胞与基因治疗(CGT)及大分子药物领域,致力于为客户提供从研发、生产、销售到技术服务的原代细胞产品一站式解决方案。
公司以构建“生物样本—技术服务—产品”三位一体的业务闭环为核心战略,依托高标准样本资源、专业化合规服务与特色产品体系,加速客户从研发到商业化的全过程,立志成为全球生物医药产业链中值得信赖的核心合作伙伴。目前,公司已建成总面积超3000平方米的研发与GMP生产基地。旗下全资子公司上海合佑生生物科技有限公司已通过GB/T 19001-2016/ISO 9001:2015质量管理体系认证,并荣获“上海市高新技术企业”与“上海市专精特新中小企业”称号。
企业始终秉持以“人才为基础,质量为先,创新为本”的核心价值观,坚持技术创新驱动,引领国产创新的行业新标准,为中国创新药发展和超越提供坚实的基础。




